Обикновени аминокиселини и синтез на протеини
Аминокиселините, които се появяват най-често в протеиновите структури на живите организми, се наричат обикновени аминокиселини или протеиногени. Въпреки че в природата са известни повече от 500 вида аминокиселини, това, което наричаме обикновени, са само двадесет. Наред с тях има и по-редки, наричани от време на време такива, които обикновено произтичат от метаболизма на обикновените след включването им в протеиновата верига. В колаген, например, лизин и пролин, две обикновени аминокиселини, се намират в хидроксилираната форма (хидроксипролин и хидроксилизин).
Повечето от другите необичайни аминокиселини са съставени главно от ензими и хормони на протеинова природа, или по-добър пептид (не забравяйте, че за да се разглежда като такъв, протеинът трябва да се състои от повече от 100 аминокиселини, докато да се образува олиго и полипептид е достатъчен от 2 до 9 и от 10 до 100).
Сред 20-те обикновени аминокиселини, които помним
Аланин, аргинин, аспарагин, аспарагинова киселина, цистеин, глицин, глутаминова киселина, глутамин, хистидин, изолевцин, левцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин, валин
Примери за не-обикновени аминокиселини са: \ t
карнитин (участва в транспорта на дълговерижни мастни киселини в митохондрия, където те се използват за производство на енергия);
орнитин, цитрулин и хомоцистеин (те участват в метаболизма на аминокиселини - цикъл на урея);
хидроксипролин и хидроксилизин (включени в състава на колаген и някои протеини);
саркозин (или метилглицин).
Някои аминокиселини могат също да имат търговско или фармакологично значение.
- Натриевият глутамат се използва в хранително-вкусовата промишленост като овкусител (виж запасния куб).
- L-дихидроксифенилаланин (L-DOPA) е лекарство, използвано за лечение на болестта на Паркинсон.
- 5-хидрокситриптофан (5-HTP) е бил използван за лечение на неврологични симптоми, свързани с фенилкетонурия (наследствено метаболитно заболяване, което предотвратява използването на фенилаланин, незаменима аминокиселина, поради специфични ензимни дефицити, натрупването на фенилаланин в тъканите е отговорен за сериозни увреждания на кожата и неврологичното ниво).
Растенията и бактериите са способни да произвеждат определени аминокиселини, които могат да бъдат намерени в пептидните антибиотици, като низин и аламетицин.
Съществени аминокиселини
Някои от 20-те обикновени аминокиселини се наричат съществени, тъй като не могат да бъдат синтезирани от организма от други съединения, а трябва да се приемат с храна.
За хората това са фенилаланин, левцин, изолевцин, лизин, метионин, треонин, триптофан, валин и при деца - хистидин и аргинин.
Обикновени аминокиселини, химични характеристики
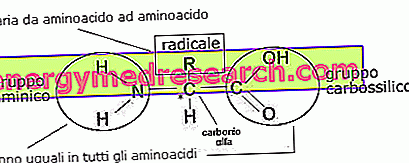
Въз основа на химичните характеристики на R радикал (група от атоми, които образуват не много дълга верига), аминокиселините могат да бъдат разделени на няколко категории.
Аминокиселини с R аполар (неспособни да образуват водородни връзки):
с алифатна верига: аланин, левцин, изолевцин, валин, пролин
с ароматна верига: фенилаланин, триптофан
с верига, съдържаща серен атом: метионин
Аминокиселини с полярна R:
с ОН група: серин, треонин, тирозин
с SH група: цистеин
с CO-NH2 група : аспарагин, глутамин
с Н: глицин (единствената нехирална аминокиселина)
Аминокиселини с основен R:
лизин, аргинин, хистидин
Аминокиселини с киселина R:
глутаминова киселина, аспарагинова киселина